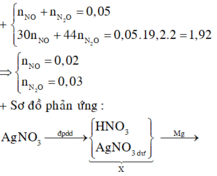
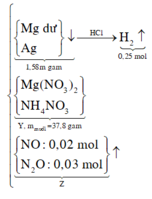
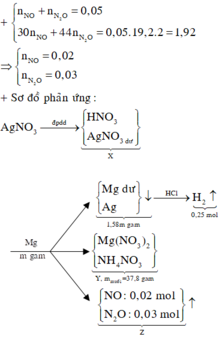
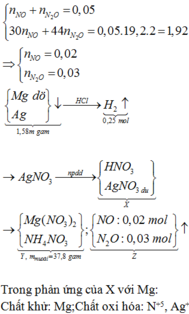
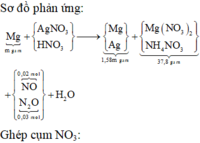
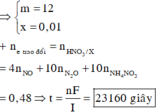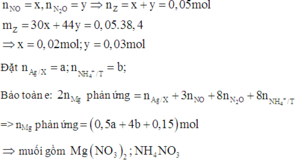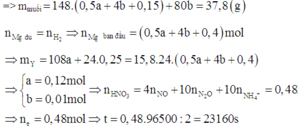Điện phân dung dịch chứa A g N O 3 với điện cực trơ trong thời gian t (s), cường độ dòng điện 2A thu được dung dịch X. Cho m gam bột Mg vào dung dịch X, sau phản ứng xảy ra hoàn toàn thu được 2,4 gam hỗn hợp kim loại; 3,36 lít hỗn hợp khí Z(đktc) gồm NO và N 2 O có tỉ khối đối với H 2 là và dung dịch Y chứa 25,56 gam muối. Cho toàn bộ hỗn hợp bột kim loại trên tác dụng với dung dịch HCl dư thu được 0,224 lit khí H 2 (dktc). Giá trị của t là
A. 11097,5
B. 28950,1
C. 23167,6
D. 20196,4