Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Khi cho từ từ HCl và X, đã có phương trình tạo khí
H+ + HCO3- → CO2 + H2O
Dung dịch Y không thể chứa OH- , CO32-. Vậy Y chứa KCl 0,5 mol (BTNT cho Cl) và KHCO3 y mol.
Cho y phản ứng với Ba(OH)2 dư:
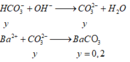
ĐLBKL cho K ta có n(KOH) ban đầu = 0,4x= 0,5 +y = 0,7 => y = 1,75

Đáp án D
Nhỏ từ từ axit vào dung dịch X ⇒ dung dịch Y.
⇒ Y chứa KCl và KHCO3.
Cho Y + dung dịch Ba(OH)2 dư ⇒ có phản ứng.
KHCO3 + Ba(OH)2 → BaCO3 + KOH + H2O.
+ Mà nKHCO3 = nBaCO3 = 0,2 mol.
+ Bảo toàn Cl ⇒ nKCl = nHCl = 0,5 mol.
⇒ Bảo toàn K ⇒ nKOH = nKCl + nKHCO3 = 0,7 mol.
⇒ CM KOH = 0 , 7 0 , 4 = 1,75M

Đáp án D
Nhỏ từ từ axit vào dung dịch X ⇒ dung dịch Y.
⇒ Y chứa KCl và KHCO3.
Cho Y + dung dịch Ba(OH)2 dư ⇒ có phản ứng.
KHCO3 + Ba(OH)2 → BaCO3 + KOH + H2O.
+ Mà nKHCO3 = nBaCO3 = 0,2 mol.
+ Bảo toàn Cl ⇒ nKCl = nHCl = 0,5 mol.
⇒ Bảo toàn K ⇒ nKOH = nKCl + nKHCO3 = 0,7 mol.
⇒ CM KOH = 0 , 7 0 , 4 = 1,75M

Đáp án C
Gọi số mol mỗi ion NH4+, K+, CO32-, SO42- trong mỗi phần lần lượt là x, y, z , t mol
Phần 1: Ba2++ CO32-→ BaCO3
z z
Ba2++ SO42- → BaSO4
t t
NH4++ OH-→ NH3+ H2O
x x = 0,3 mol
mkết tủa= mBaCO3+ mBaSO4= 197z+233t= 43 suy ra t= 0,1 mol
Phần 2: 2H++ CO32- → CO2+ H2O
z mol z mol= 0,1
Định luật bảo toàn điện tích: x+y=2z+ 2t suy ra y= 0,1 mol
mmuối= (18x+ 39y+60z+96t).2= 49,8 gam

Đáp án C
Bảo toàn nguyên tố cho cacbon ta có
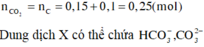
Thứ tự các phản ứng xảy ra khi cho từ từ dung dịch H+ vào dung dịch X là
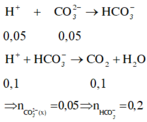
Các phản ứng tạo thành các chất trong dung dịch X
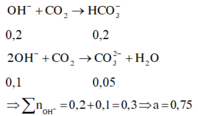


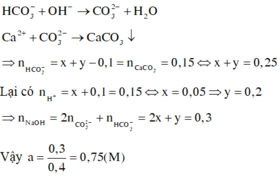
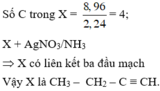


Chọn đáp án D